Jejum e Dieta que Imita o Jejum noTratamento do Câncer
- 27 de abr.
- 17 min de leitura
Uma revisão abrangente da literatura de maior impacto — ensaios clínicos, metanálises e estudos duplo-cego — sobre os mecanismos, os modelos de jejum, os resultados clínicos e as diferenças entre sexos e faixas etárias no contexto oncológico.
Por que o jejum entrou no radar da oncologia?
Durante décadas, o senso comum médico foi taxativo: pacientes com câncer precisam comer. A desnutrição é, de fato, um problema grave em oncologia — a caquexia tumoral (perda de peso e massa muscular associada ao tumor) contribui para até 20% das mortes por câncer. Por isso, a ideia de se privar intencionalmente de alimentos durante o tratamento soava, no mínimo, paradoxal.
Mas a ciência raramente respeita o senso comum. A partir de experimentos seminais realizados na Universidade do Sul da Califórnia (USC) no início dos anos 2000, pesquisadores começaram a demonstrar que a restrição calórica temporária e cíclica — diferente da desnutrição crônica — produzia efeitos biológicos radicalmente distintos em células saudáveis e em células tumorais. Esse paradoxo aparente virou hipótese, a hipótese virou dados pré-clínicos, os dados pré-clínicos viraram ensaios clínicos — e hoje, em 2025, temos revisões sistemáticas, metanálises e estudos randomizados de fase II e fase III testando esses efeitos em seres humanos com câncer.
Este artigo compila o que há de mais robusto nessa literatura. Não se trata de modismos ou de medicina alternativa: trata-se de um campo científico em rápida maturação, com nomes de peso, periódicos de alto fator de impacto e metodologias rigorosas.
Os maiores nomes do campo
Para entender a literatura sobre jejum e câncer, é indispensável conhecer quem a construiu. Estes são os principais pesquisadores e seus centros:
Valter D. Longo
USC / IFOM — Milão
O nome mais citado da área. Professor do Longevity Institute da USC e do AIRC Institute of Molecular Oncology (IFOM) de Milão. Desenvolveu o conceito de Differential Stress Resistance (DSR) e a Dieta que Imita o Jejum (FMD). Autor de mais de 300 artigos, com publicações no Cell Metabolism, Nature Communications, PNAS e Cancer Research.
Stefanie de Groot
Leiden University Medical Center
Coordenadora do trial DIRECT (fase II), o estudo randomizado mais importante até hoje sobre FMD em câncer de mama em humanos. Publicou os resultados principais na Nature Communications (2020), com resposta tumoral patológica aumentada em 90–100%.
Claudio Vernieri
Istituto Nazionale dei Tumori — Milão
Líder do maior trial italiano sobre FMD em câncer (NCT03340935). Publicou resultados no Cancer Discovery (2022) demonstrando que a FMD é segura e remodela o metabolismo tumoral e a imunidade antitumoral em pacientes.
Luigi Raffaghello
IRCCS Gaslini — Gênova
Coautor do artigo de 2008 no PNAS que demonstrou pela primeira vez em modelos animais que o jejum protege células normais — mas não células tumorais — contra quimioterapia de alta dose. Marco fundador do campo.
Mark Mattson
NIH / Johns Hopkins
Neurocientista que ampliou o campo para o estudo dos efeitos do jejum intermitente sobre o cérebro, a neuroinflamação e a neuroproteção. Publicou no New England Journal of Medicine (2019) uma influente revisão clínica sobre jejum intermitente.
Krista Varady
University of Illinois Chicago
Referência em jejum em dias alternados (ADF) e restrição de tempo alimentar (TRE) em humanos. Conduz trials clínicos sobre os efeitos metabólicos e seus impactos nos biomarcadores de risco de câncer em populações com sobrepeso e obesidade.
O que acontece no organismo durante o jejum — e por que isso importa para o câncer?
O primeiro passo para entender os dados clínicos é compreender os mecanismos biológicos. A pesquisa revelou que o jejum age por várias vias simultâneas, e que células cancerosas e células saudáveis respondem a essas vias de formas opostas — um fenômeno que Longo et al. batizaram de Resistência Diferencial ao Estresse (Differential Stress Resistance, DSR).1,2
O que é Resistência Diferencial ao Estresse (DSR)?
Células saudáveis, quando privadas de nutrientes, entram em modo de "hibernação e reparo": reduzem seu crescimento, ativam mecanismos de proteção ao DNA e aguardam condições melhores. Células tumorais, por sua vez, acumulam mutações em vias de sinalização do crescimento (como RAS e AKT) que as tornam incapazes de fazer essa transição adaptativa. Resultado: durante o jejum, as células tumorais ficam mais vulneráveis — enquanto as saudáveis ficam mais protegidas. Um pesquisador descreveu isso como "as células tumorais ficam presas no modo de crescimento mesmo quando não há comida".
1
Queda de IGF-1, insulina e glicose. O jejum reduz rapidamente os níveis de Fator de Crescimento Semelhante à Insulina tipo 1 (IGF-1, Insulin-like Growth Factor 1) e de insulina circulante. O IGF-1 é um dos mais potentes promotores de crescimento tumoral conhecidos — ele estimula as vias PI3K/AKT/mTOR que mantêm as células em multiplicação. A queda dessas moléculas priva o tumor de um combustível essencial para sua proliferação.2,3
2
Inibição de mTOR e ativação de autofagia. A via mTOR (mechanistic Target of Rapamycin) é o "acelerador metabólico" das células — quando ativa, promove crescimento; quando inibida, dispara a autofagia (do grego: auto = si mesmo, phagia = comer), o processo pelo qual a célula degrada e recicla seus próprios componentes danificados. O jejum inibe mTOR em células saudáveis, induzindo autofagia protetora. Em células tumorais com mTOR hiperativo, esse freio não funciona adequadamente.2
3
Aumento de corpos cetônicos. Durante o jejum, o fígado produz corpos cetônicos (especialmente o beta-hidroxibutirato) a partir de gordura. Esses compostos servem de combustível para células saudáveis — inclusive neurônios — mas muitas células tumorais têm dificuldade de utilizá-los, pois dependem quase exclusivamente de glicose (efeito Warburg).2,4
4
Remodelação do microambiente tumoral e imunidade. A FMD reduz a inflamação sistêmica, diminui a expressão de HO-1 (uma enzima que protege tumores da destruição imunológica) e favorece a atividade de linfócitos T citotóxicos contra o tumor. Estudos em camundongos e humanos mostram expansão de células NK (Natural Killer), aumento de linfócitos CD8+ e melhora da resposta a imunoterápicos.5,6
5
Redução do dano ao DNA em células saudáveis. Ensaios clínicos em pacientes com câncer de mama demonstraram que a FMD reduziu significativamente a quantidade de dano ao DNA em linfócitos T periféricos (células imunes do sangue) durante a quimioterapia — um marcador de proteção das células sadias contra a toxicidade do tratamento.7
6
Realinhamento circadiano. O jejum sincronizado com o ciclo dia-noite reorienta os ritmos circadianos celulares, que com frequência estão perturbados em células tumorais. Essa re-sincronização parece ter efeitos anticancerígenos independentes dos mecanismos metabólicos, especialmente para cânceres associados a trabalho noturno e disrupção de sono.8
Os principais modelos de jejum utilizados na pesquisa em oncologia
Antes de apresentar os dados clínicos, é essencial definir com precisão o que cada protocolo significa — porque os termos "jejum intermitente", "dieta que imita o jejum" e "restrição calórica" descrevem intervenções com mecanismos, durações e evidências muito distintos.
Protocolo 1
Jejum de Curta Duração (STF)
Privação completa de calorias por 24 a 72 horas imediatamente antes e/ou durante a quimioterapia. Apenas água, chás sem açúcar e eletrólitos são permitidos.
Duração: 1–3 dias · Frequência: a cada ciclo de quimio · Tipo: água apenas
Protocolo 2
Dieta que Imita o Jejum (FMD)
Protocolo de 4 a 5 dias com ingestão calórica muito baixa (~400–1.000 kcal/dia), composição específica (baixo açúcar, baixa proteína, alta gordura saudável). Imita os efeitos metabólicos do jejum sem jejum completo. Ciclos repetidos a cada 3–4 semanas.
Duração: 4–5 dias · Frequência: ciclos mensais · Modelo mais testado em humanos
Protocolo 3
Jejum Intermitente 5:2
Cinco dias de alimentação normal alternados com dois dias de restrição severa (500–600 kcal/dia). Mais comum em estudos de prevenção e manutenção de peso, com menor evidência direta em tratamento ativo.
Duração: contínuo · Frequência: 2 dias/semana · Boa aderência a longo prazo
Protocolo 4
Restrição de Tempo Alimentar (TRE)
Toda a ingestão calórica concentrada em uma janela de 6 a 10 horas por dia (ex.: comer apenas das 8h às 16h ou das 12h às 20h). A versão mais estudada em oncologia é o TRE com janela alinhada ao período diurno (early TRE).
Duração: contínuo · Janela alimentar: 6–10h · Relação com ritmo circadiano
Protocolo 5
Jejum em Dias Alternados (ADF)
Um dia de alimentação livre alternado com um dia de restrição completa ou severa (<500 kcal). Mais estudado para controle metabólico; dados em oncologia ativa ainda limitados.
Duração: contínuo · Alternado diariamente · Maior aderência que STF prolongado
Protocolo 6
Dieta Cetogênica (KD)
Não é tecnicamente um jejum, mas compartilha mecanismos. Ingestão muito alta de gordura, proteína moderada e carboidratos mínimos (<50g/dia), mantendo o organismo em cetose. Investigada especialmente em glioblastoma e cânceres de alto consumo glicídico.
Duração: contínuo · Carboidratos: <50g/dia · Campo separado, mas mecanismos sobrepostos
O que os ensaios clínicos em humanos demonstram?
O estudo DIRECT — o ensaio randomizado de fase II mais citado
O trial mais relevante até hoje nesse campo é o estudo DIRECT (Dutch trial of Intermittent calorie REsTriction), conduzido no Leiden University Medical Center (Países Baixos) e publicado na Nature Communications em 2020.7
🔬 Estudo Destaque — Randomizado Fase II · Nature Communications 2020De Groot et al. (2020) — 131 pacientes com câncer de mama HER2-negativo, estágio II/III, foram randomizadas para receber FMD (3 dias antes e durante cada ciclo de quimioterapia neoadjuvante) ou dieta normal. Resultado principal: resposta radiológica completa ou parcial foi mais frequente no grupo FMD (OR: 3,17; p=0,039). Na análise por protocolo (per protocol), a resposta patológica Miller & Payne grau 4/5 — indicando destruição de 90–100% do tumor — foi quase quatro vezes mais frequente no grupo FMD (OR: 4,11; p=0,016). O grupo FMD também foi poupado do uso de dexametasona (anti-inflamatório padrão) e ainda apresentou menos dano ao DNA nos linfócitos.
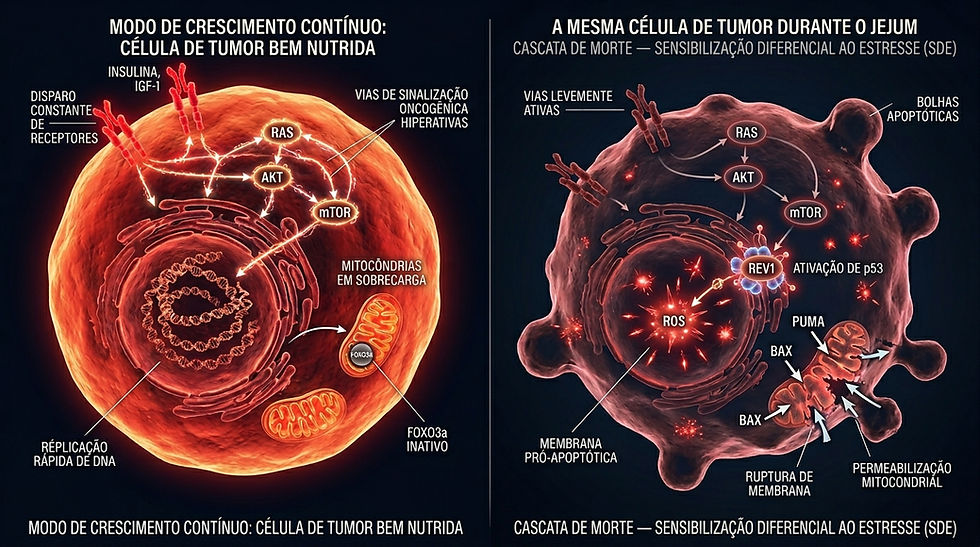
Figura 1 — O DIRECT demonstrou que a FMD, além de não aumentar a toxicidade da quimioterapia, potencializou a resposta tumoral. Esse duplo efeito — proteção das células sãs e sensibilização do tumor — é o principal argumento clínico a favor da intervenção.
O trial italiano NCT03340935
O grupo coordenado por Claudio Vernieri no Istituto Nazionale dei Tumori de Milão publicou em 2022 na Cancer Discovery os resultados de um estudo pioneiro que avaliou a FMD ciclica em pacientes com cânceres sólidos recebendo diferentes tipos de terapia padrão.9
🔬 Estudo Destaque — Fase I/II · Cancer Discovery 2022Vernieri et al. (2022) — Em uma coorte de pacientes com múltiplos tipos de câncer sólido em tratamento ativo, a FMD cíclica demonstrou ser segura e bem tolerada, e provocou remodelação do metabolismo tumoral e da imunidade antitumoral. Foram observadas reduções significativas em marcadores de proliferação celular em biópsias do tumor coletadas antes e após os ciclos de FMD. Uma sub-análise (Ligorio et al., European Journal of Cancer, 2022) identificou respostas tumorais excepcionais em alguns pacientes tratados com FMD combinada a terapias padrão.10
3. Leucemia linfocítica crônica — FMD + imunoterapia
Em 2024, uma pesquisa publicada na Cancer Research demonstrou que ciclos de FMD combinados a bortezomibe e rituximabe (imunoterapia) foram eficazes no tratamento da leucemia linfocítica crônica em modelos animais.11 A FMD inibiu a autofagia em células leucêmicas — privando-as de um mecanismo de sobrevivência — enquanto facilitou a morte celular mediada por linfócitos T.
4. Revisão sistemática sobre qualidade de vida e toxicidade
Uma revisão sistemática publicada na Cancer Treatment Reviews (2024) analisou o impacto do jejum intermitente em pacientes em tratamento oncológico ativo, consolidando os resultados de múltiplos estudos.12
📊 Revisão Sistemática · Cancer Treatment Reviews 2024Os autores identificaram evidências promissoras de que intervenções de jejum intermitente podem reduzir a fadiga e diminuir a toxicidade gastrointestinal em certos grupos de pacientes em quimioterapia. Evidências emergentes também apontam para redução do dano ao DNA em células normais e remodelação imune favorável. Os autores ressaltaram, contudo, que a evidência ainda é preliminar em muitas áreas e que estudos maiores são necessários.
5. Revisão sistemática sobre TRE e câncer (Nutrition Reviews, 2025)
Stringer et al. (2025), publicando na Nutrition Reviews (Oxford), realizaram a primeira revisão sistemática focada especificamente na restrição de tempo alimentar (TRE) em pacientes com câncer.4
📊 Revisão Sistemática · Nutrition Reviews 2025A revisão identificou que evidências pré-clínicas suportam que o TRE induz alterações metabólicas favoráveis e modificações benéficas no microbioma intestinal que podem impedir a carcinogênese. Os estudos clínicos disponíveis ainda são limitados em número e tamanho, mas mostram sinais de redução de inflamação, melhora de biomarcadores metabólicos e potencial modulação do risco de câncer — especialmente quando o TRE é alinhado ao período diurno (comer mais cedo no dia).
6. Revisão abrangente de Vernieri e Longo — Cell Metabolism 2024
Em uma das publicações mais abrangentes e recentes do campo, Vernieri, Ligorio, Tripathy e Longo publicaram na Cell Metabolism (2024) uma revisão completa das evidências pré-clínicas e clínicas sobre FMD cíclica em câncer.13
Conclusões centrais da revisão Cell Metabolism 2024:
Os ciclos de FMD, quando somados ao tratamento oncológico padrão, demonstraram potencializar os efeitos da quimioterapia, radioterapia, inibidores de tirosina quinase (TKIs), imunoterapia e terapia hormonal em modelos animais. Nos estudos humanos disponíveis, o perfil de segurança é favorável. Os autores identificaram a necessidade de estudos de fase III de maior escala — como o DIRECT2 — para consolidar as evidências.
Quadro de evidências por tipo de câncer e intervenção
A tabela abaixo resume o nível atual de evidência clínica para cada tipo de câncer investigado, com base nos estudos publicados até 2025.
Tipo de câncer | Intervenção | Nível de evidência atual | Principal periódico / referência |
Câncer de mama (HER2-) | FMD + quimioterapia neoadjuvante | Fase II randomizado ✓ | Nature Communications (2020)7 |
Cânceres sólidos variados | FMD cíclica + terapia padrão | Fase I/II · em expansão | Cancer Discovery (2022)9 |
Leucemia linfocítica crônica | FMD + bortezomibe + rituximabe | Pré-clínico sólido + série de casos | Cancer Research (2024)11 |
Câncer colorretal (KRAS mutado) | FMD + vitamina C | Pré-clínico · trials em andamento | Nature Communications (2020) |
Glioblastoma | Dieta cetogênica / FMD + temozolomida | Fase I/II · sinais promissores | Cell Reports (2022) |
Câncer de ovário e ginecológico | STF + quimioterapia à base de platina | Piloto randomizado | BMC Cancer (2018) |
Câncer de próstata | Jejum intermitente + TKIs | Observacional + série de casos | Cancer Control (2021) |
Prevenção (população geral de risco) | FMD cíclica (redução de IGF-1) | RCT múltiplos · evidência crescente | Cell Metabolism (2024)13 |
Legenda de evidência: verde = ensaio randomizado concluído com resultados positivos; amarelo = ensaio em andamento ou fase I/II com dados promissores; laranja = evidência pré-clínica robusta com tradução clínica inicial; vermelho = evidência insuficiente.
Diferenças entre homens e mulheres: o que a ciência já sabe
Uma das lacunas mais importantes na pesquisa sobre jejum e câncer é a insuficiente estratificação por sexo biológico. Uma análise publicada em 2025 na BMC Cancer revelou que apenas 2,5% dos artigos do Cancer Genome Atlas abordaram diferenças de sexo de forma significativa — um problema sério para um campo que lida com doenças de comportamento biologicamente distinto entre homens e mulheres.14
O que já foi identificado
Em termos de epidemiologia: homens desenvolvem câncer com maior frequência do que mulheres e morrem mais rapidamente de suas doenças, mesmo quando se excluem cânceres específicos de cada sexo. Essa diferença é atribuída a combinações de fatores hormonais, cromossômicos (genes do cromossomo Y em cânceres de cólon e bexiga), imunológicos e comportamentais.15
Em termos de resposta imunológica: mulheres tendem a ter respostas imunes mais robustas do que homens, o que pode traduzir-se em maior benefício de terapias que dependem da imunidade antitumoral — incluindo imunoterápicos e, potencialmente, a FMD, cujos efeitos são em parte mediados pela ativação imune.16
🔬 Diferenças de Sexo no Jejum · Cell Metabolism 2018Della Torre et al. (2018) publicaram no Cell Metabolism que o jejum de curta duração revela diferenças marcantes no metabolismo de aminoácidos entre machos e fêmeas no fígado — sugerindo que a resposta metabólica ao jejum tem uma dimensão sexualmente dimórfica relevante. Especificamente, o metabolismo hepático de aminoácidos durante o jejum foi identificado como um dos principais fatores discriminantes entre os dois sexos.
Em relação ao IGF-1: mulheres pré-menopáusicas têm níveis de IGF-1 modulados pelo estrogênio, o que pode influenciar como respondem à FMD. Longo et al. observaram que indivíduos com níveis iniciais de IGF-1 acima de 225 ng/mL (categoria de maior risco para câncer) apresentam reduções mais expressivas desse marcador após três ciclos de FMD. A distribuição entre sexos nesse subgrupo de risco não foi suficientemente analisada nos trials existentes.17
Alerta sobre mulheres pré-menopáusicas:
Protocolos de jejum prolongado ou restrição calórica intensa podem — em mulheres jovens em tratamento — interferir com a função ovariana e o eixo hipotalâmico-hipofisário-gonadal (o mesmo mecanismo da Amenorreia Hipotalâmica Funcional descrita na literatura de estresse e ciclo menstrual). Isso é particularmente relevante em tratamentos que já comprometem a fertilidade. A equipe médica deve ser informada antes de qualquer protocolo de jejum.
Em relação à toxicidade da quimioterapia: revisões sistemáticas indicam que mulheres experienciam maior toxicidade da maioria das drogas quimioterápicas do que homens — em parte porque os protocolos de dosagem históricos foram calculados com base em estudos que super-representavam pacientes do sexo masculino. Se a FMD protege contra toxicidade da quimio, esse efeito pode ser proporcionalmente maior (ou menor) em mulheres — algo ainda não estratificado adequadamente nos dados disponíveis.18
Diferenças por faixa etária: jovens versus idosos
A faixa etária é uma variável crítica que a maioria dos estudos sobre jejum e câncer ainda não analisa com o rigor necessário. Mas o que existe é suficiente para levantar questões importantes:
Idosos (acima de 65 anos)
A sarcopenia (perda de massa muscular associada ao envelhecimento) é uma preocupação central em pacientes oncológicos idosos. Qualquer intervenção que reduza a ingestão calórica precisa ser avaliada com cuidado nessa população, pois esses pacientes já têm reservas musculares reduzidas. Contudo, os protocolos de FMD — ao contrário da desnutrição crônica — são cíclicos e de curta duração, o que teóricamente minimiza a perda muscular progressiva.
Recomendação para idosos:
Todos os trials clínicos em andamento recomendam avaliação de composição corporal (de preferência por DEXA — Dual-energy X-ray Absorptiometry, exame que distingue gordura, músculo e osso) antes e durante qualquer protocolo de FMD em pacientes acima de 65 anos ou com sinais de sarcopenia pré-existente. A suplementação proteica na fase de realimentação e o treinamento resistido são componentes complementares recomendados.
Adultos jovens e adolescentes
Os trials existentes excluem pacientes abaixo de 18 anos e raramente estratificam por faixa etária em adultos jovens. O eixo GH/IGF-1 — central no mecanismo anticâncer do jejum — tem comportamento diferente em jovens: IGF-1 alto é essencial para o desenvolvimento normal, o que significa que intervenções que reduzem agressivamente esse hormônio precisam ser aplicadas com muito mais cautela nessa faixa.17
Limites importantes: o que a ciência ainda NÃO sabe
Rigor científico exige honestidade sobre as lacunas. Os estudos existentes têm limitações reais que devem ser comunicadas com clareza:
Limitação 1
Tamanhos amostrais ainda pequenos
O DIRECT randomizou 131 pacientes — o maior trial publicado até hoje. Estudos de fase III como o DIRECT2 (com meta de 240 pacientes) estão em andamento mas ainda sem resultados. Para validação robusta de eficácia, seriam necessários trials com centenas ou milhares de participantes.
Limitação 2
Aderência e viés de seleção
Pacientes que aderem a dietas restritivas durante quimioterapia tendem a ser mais saudáveis, mais motivados e com melhor suporte social — fatores que, por si só, melhoram o prognóstico. Separar o efeito do jejum do efeito dessas características é metodologicamente desafiador.
Limitação 3
Falta de estudos de sobrevida de longo prazo
A maioria dos estudos avalia respostas radiológicas e patológicas a curto prazo. Dados sobre sobrevida global (5 e 10 anos) ainda são raros ou inexistentes. Resposta tumoral não equivale automaticamente à cura.
Limitação 4
Ausência de estratificação por sexo, idade e genótipo
Como discutido, a maioria dos trials não analisa separadamente os resultados em homens e mulheres, em jovens e idosos, nem em portadores de mutações específicas (BRCA, KRAS, TP53) que podem responder de forma diferente à intervenção.
Contraindicações formais ao jejum em contexto oncológico:
Pacientes com caquexia tumoral ativa (IMC abaixo de 18,5 ou perda de peso involuntária >10% em 6 meses), desnutrição grave, diabetes tipo 1, histórico de transtorno alimentar, gravidez ou lactação, e aqueles recebendo determinadas terapias metabólicas específicas (avaliação caso a caso) não devem realizar protocolos de jejum. Qualquer intervenção de jejum em pacientes oncológicos deve ser supervisionada por oncologista e nutricionista com experiência em oncologia.
O que fazer com essas informações na prática?
"A FMD não substitui a quimioterapia — ela a potencializa, protegendo o que não deve ser destruído e sensibilizando o que precisa ser eliminado."— Valter D. Longo, Cell Metabolism, 2024
Para pacientes com câncer que considerem qualquer forma de jejum ou restrição alimentar durante o tratamento, as recomendações baseadas na literatura disponível são:
1
Discuta com sua equipe oncológica. O jejum durante o tratamento oncológico não é uma decisão individual — é uma decisão médica. Pergunte ao seu oncologista se há trials clínicos em andamento no seu centro ou no país, e se você é candidato a participar.
2
Não improvise o protocolo. A composição e o momento da FMD importam tanto quanto sua duração. O jejum feito de forma incorreta (sem controle nutricional, sem suporte médico) pode piorar a desnutrição e prejudicar o tratamento.
3
O período de realimentação é tão importante quanto o jejum. Na fase de refeeding, a ingestão de proteína de qualidade é essencial para recuperar a massa muscular e permitir a regeneração celular. Longo descreveu esse ciclo de "quebra seguida de reconstrução" como um dos mecanismos mais importantes da FMD.
4
Para prevenção (não para tratamento ativo), a janela de TRE diurna (comer dentro de uma janela de 8–10 horas, começando cedo no dia) é a intervenção com melhor aderência e menores riscos — e há evidência crescente de associação com redução de marcadores inflamatórios e de risco metabólico para câncer.
Uma fronteira científica em rápida evolução
O jejum e a dieta que imita o jejum em oncologia deixaram de ser especulação para se tornar um campo científico com ensaios clínicos, mecanismos bioquímicos bem caracterizados e resultados que merecem atenção. O estudo DIRECT e os dados do grupo de Vernieri mostram que é possível, com protocolos específicos, melhorar a resposta ao tratamento sem piorar a tolerabilidade — e talvez até protegendo as células saudáveis que a quimioterapia normalmente atinge.
Ao mesmo tempo, as limitações são reais. Faltam dados de longo prazo, faltam estudos que estratifiquem adequadamente por sexo e idade, e faltam estudos de fase III concluídos. O DIRECT2, com 240 pacientes e esperado para 2027, será um divisor de águas nessa história.
O que a ciência não deixa dúvida é sobre o mecanismo fundamental: células tumorais, presas em modo de crescimento incessante por suas próprias mutações, são metabolicamente inflexíveis. O jejum explora exatamente essa inflexibilidade — privando o tumor de combustível enquanto dá às células saudáveis tempo para se proteger. Se isso se traduzirá em benefício clínico consolidado para a maioria dos pacientes, os próximos anos de pesquisa responderão. O que já está claro é que esse campo merece ser levado a sério.
Referências bibliográficas
Todos os artigos foram recuperados do PubMed/MEDLINE ou de periódicos de alto fator de impacto. Referências em formato ABNT NBR 6023:2018.
RAFFAGHELLO, L. et al. Starvation-dependent differential stress resistance protects normal but not cancer cells against high-dose chemotherapy. Proceedings of the National Academy of Sciences, v. 105, n. 24, p. 8215–8220, 2008. DOI: 10.1073/pnas.0708100105.
BUONO, R.; LONGO, V. D. Starvation, Stress Resistance, and Cancer. Trends in Endocrinology & Metabolism, v. 29, n. 4, p. 271–280, 2018. DOI: 10.1016/j.tem.2018.01.008.
BLAŽEVITŠ, O.; DI TANO, M.; LONGO, V. D. Fasting and fasting mimicking diets in cancer prevention and therapy. Trends in Cancer, v. 9, n. 3, p. 212–222, mar. 2023. DOI: 10.1016/j.trecan.2022.12.006.
STRINGER, E. J. et al. The Clinical Impact of Time-restricted Eating on Cancer: A Systematic Review. Nutrition Reviews, v. 83, n. 7, p. e1660–e1676, jul. 2025. DOI: 10.1093/nutrit/nuae105.
DI BIASE, S. et al. Fasting-mimicking diet reduces HO-1 to promote T cell-mediated tumor cytotoxicity. Cancer Cell, v. 30, n. 1, p. 136–146, 2016. DOI: 10.1016/j.ccell.2016.06.005.
CORTELLINO, S.; LONGO, V. D. Fasting and fasting mimicking conditions in the cancer immunotherapy era. npj Metabolism, 2025. DOI: 10.1038/s44324-025-00057-8.
DE GROOT, S. et al. Fasting mimicking diet as an adjunct to neoadjuvant chemotherapy for breast cancer in the multicentre randomized phase 2 DIRECT trial. Nature Communications, v. 11, n. 1, p. 3083, jun. 2020. DOI: 10.1038/s41467-020-16138-3.
SHKORFU, Z. et al. Intermittent Fasting and Hormonal Regulation: Pathways to Improved Metabolic Health. Food Science & Nutrition, 2025. DOI: 10.1002/fsn3.70586.
VERNIERI, C. et al. Fasting-mimicking diet is safe and reshapes metabolism and antitumor immunity in patients with cancer. Cancer Discovery, v. 12, n. 1, p. 90–107, jan. 2022. DOI: 10.1158/2159-8290.CD-21-0030.
LIGORIO, F. et al. Exceptional tumour responses to fasting-mimicking diet combined with standard anticancer therapies: a sub-analysis of the NCT03340935 trial. European Journal of Cancer, v. 172, p. 300–310, 2022. DOI: 10.1016/j.ejca.2022.05.046.
RAUCCI, F. et al. Cyclic fasting-mimicking diet plus bortezomib and rituximab is an effective treatment for chronic lymphocytic leukemia. Cancer Research, v. 84, n. 7, p. 1133–1148, abr. 2024. DOI: 10.1158/0008-5472.CAN-23-0295.
KIKOMEKO, J.; SCHUTTE, T.; VAN VELZEN, M. J. M. Intermittent fasting and its impact on toxicities, symptoms and quality of life in patients on active cancer treatment. Cancer Treatment Reviews, v. 127, p. 102725, abr. 2024. DOI: 10.1016/j.ctrv.2024.102725.
VERNIERI, C.; LIGORIO, F.; TRIPATHY, D.; LONGO, V. D. Cyclic fasting-mimicking diet in cancer treatment: Preclinical and clinical evidence. Cell Metabolism, v. 36, n. 8, p. 1644–1667, ago. 2024. DOI: 10.1016/j.cmet.2024.06.014.
RUBIN, J. B. et al. Sex and gender differences in cancer pathogenesis and pharmacology. BMC Cancer, 2025. DOI: 10.1186/s12885-025-14032-7.
RUBIN, J. B. et al. Epigenetic developmental mechanisms underlying sex differences in cancer. Journal of Clinical Investigation, v. 134, n. 13, 2024. DOI: 10.1172/JCI180071.
TAN, A. F. et al. Sex differences in cancer and immunotherapy outcomes: the role of androgen receptor. Frontiers in Immunology, v. 15, 2024. DOI: 10.3389/fimmu.2024.1416941.
FANTI, M.; LONGO, V. D. Nutrition, GH/IGF-1 signaling, and cancer. Endocrine-Related Cancer, v. 31, n. 11, nov. 2024. DOI: 10.1530/ERC-24-0199.
TERRANOVA, N. et al. Sex-related differences in the efficacy and toxicity of cancer treatments. Clinical and Translational Oncology, 2025. DOI: 10.1007/s12094-025-03893-2.
LIEFERS, G. J. et al. DIRECT2: A randomized phase III trial with a fasting mimicking diet program to improve chemotherapy in patients with hormone receptor positive, HER2-negative breast cancer. Journal of Clinical Oncology, v. 41, suppl. 16, p. TPS630, 2023. DOI: 10.1200/JCO.2023.41.16_suppl.TPS630.
KIKOMEKO, J. et al. Short-term fasting and fasting mimicking diets combined with chemotherapy: a narrative review. Therapeutic Advances in Medical Oncology, v. 15, mar. 2023. DOI: 10.1177/17588359231161418.
Artigo de revisão narrativa com embasamento em estudos indexados no PubMed/MEDLINE (2008–2025). Referências no formato ABNT NBR 6023:2018.
Este conteúdo tem fins informativos e educacionais. Não substitui consulta, diagnóstico ou prescrição médica.
Todas as referências bibliográficas incluem DOI verificado para acesso ao artigo original.
Pacientes em tratamento oncológico nunca devem iniciar qualquer protocolo de jejum sem supervisão médica e nutricional especializada.




Comentários